Avviso di sicurezza per dispositivo medico
Dispositivi Sleep & Respiratory Care Philips Respironics
Avviso di sicurezza 2021-05-A e Avviso di sicurezza 2021-06-A
A partire da ottobre 2023, Philips Respironics ha avviato le attività di riparazione dei dispositivi Trilogy 100/200 tramite centri di riparazione approvati da Philips in diversi paesi.
I clienti continuano ad avere la possibilità di scegliere tra la riparazione dei propri dispositivi, il riacquisto del dispositivo sotto forma di credito di vendita, gli aggiornamenti di Trilogy Evo e un programma di prestito Trilogy Evo. Il nostro obiettivo è collaborare con i nostri partner per completare la riparazione il più rapidamente possibile per i pazienti trattati con i dispositivi Trilogy 100/200 interessati.Per eventuali ulteriori domande, contatta il tuo account manager Philips Respironics.
Di seguito è riportato un aggiornamento sullo stato del nostro programma di riparazione e sostituzione per CPAP, BiPAP e dispositivi di ventilazione meccanica interessati dall'avviso di sicurezza al 31 ottobre 2024. Oltre al numero di dispositivi sostitutivi consegnati, forniamo anche una panoramica del numero di dispositivi che sarà risarcito finanziariamente e il numero di dispositivi che non possono più essere rintracciati dai fornitori di assistenza domiciliare.
1,037,268
Numero di kit di riparazione e dispositivi sostitutivi prodotti per l'Europa occidentale
28,220
Numero di dispositivi spediti a clienti in Svizzera
3,652
Compensazione finanziaria1 dei dispositivi ai fornitori di assistenza domiciliare
1,862
Dispositivi non recuperabili2
1. Alcuni vecchi dispositivi System One per l'apnea notturna non sono più prodotti e venduti da Philips. In molti casi, questi dispositivi hanno più di cinque anni. In consultazione con i fornitori di assistenza domiciliare, Philips ha concordato una soluzione per questi pazienti. Per una parte dei dispositivi usati, gli operatori domiciliari ricevono dispositivi alternativi o riparati. Inoltre, Philips offre un compenso finanziario per alcuni di questi dispositivi System One in modo che i fornitori di assistenza domiciliare possano acquistare un altro dispositivo per il paziente.
2. Gli operatori domiciliari hanno registrato una serie di dispositivi non più in uso o non più recuperabili. I fornitori di assistenza domiciliare hanno fatto del loro meglio per recuperare tutti i dispositivi e i pazienti. Partiamo dal presupposto che i dispositivi non più recuperabili non siano più in uso.
You are about to visit a Philips global content page
Continue
Tutte le informazioni per i pazienti
La sicurezza del paziente è la nostra massima priorità. Ci impegniamo a completare la riparazione per tutti i pazienti interessati per assicurarci che tutti ricevano una terapia sicura ed efficace.
Sappiamo che ogni situazione è unica a seconda del dispositivo interessato e della situazione personale. Se hai domande sul processo di riparazione o hai bisogno di ulteriore supporto dopo aver ricevuto il tuo dispositivo sostitutivo, contatta il tuo fornitore di assistenza domiciliare o il tuo medico.

Abbiamo realizzato una guida che descrive ogni passaggio del processo di correzione, così da illustrare la gestione dell'avviso di sicurezza e le azioni che ne derivano.
Ultimo aggiornamento
Aggiornamento di Philips sul avviso di sicurezza degli apparecchi Respironics
06 ottobre 2023
Risposta di Philips ai recenti articoli apparsi su alcuni media internazionali relativi all’avviso di sicurezza volontario di Respironics
27 settembre 2023
Gli ultimi risultati e conclusioni del luglio 2023 per i dispositivi per la terapia del sonno relativi all'impatto della pulizia con ozono non mostrano danni apprezzabili alla salute dei pazienti
Philips Respironics ha completato le analisi per i dispositivi per la terapia del sonno System One e DreamStation Go indicando che i composti organici volatili (COV) e le emissioni di particolato (PM) correlate alla degradazione della schiuma rientrano nei limiti di sicurezza applicabili. Sono state eseguite ulteriori valutazioni visive che confermano la bassa prevalenza di un significativo degrado della schiuma.
You are about to visit a Philips global content page
Continue
Comprendere le misure che adottiamo per garantire la sicurezza del dispositivo CPAP o BiPAP sostitutivo
Se da un lato ci adoperiamo per fornire i dispositivi sostitutivi il più rapidamente possibile, dall'altro desideriamo condividere le misure che stiamo adottando per garantire che l'uso del tuo dispositivo sostitutivo DreamStation di prima generazione sia sicuro, in modo che tu possa fidarti del tuo nuovo dispositivo.


I prodotti per la pulizia con ozono e luce UV non sono attualmente metodi di pulizia approvati per dispositivi o maschere per l'apnea del sonno e non devono essere utilizzati.
Sempre al tuo fianco

Scopri di più sull'avviso di sicurezza e registra il dispositivo interessato

Verifica i passaggi che Philips sta intraprendendo per garantire sicurezza e facilità di utilizzo
Ottobre 2022 - La valutazione di uno specialista delle apnee del sonno.
Il Prof. dr. N. de Vries, specialista in otorinolaringoiatria con un interesse particolare per la diagnosi e il trattamento delle Apnee Ostruttive del Sonno (OSA), cerca di rassicurare i pazienti interessati dall'avviso di sicurezza emesso nel giugno 2021 da Philips Respironics in relazione ad un componente presente in un certo numero di dispositivi per il trattamento delle apnee del sonno. La sua valutazione dei principali studi disponibili a livello mondiale, che hanno monitorato la salute di oltre 50.000 pazienti, conclude che non vi è alcuna differenza statisticamente significativa nel rischio complessivo di cancro associato all'uso dei dispositivi PAP Philips Respironics contenenti schiuma in poliuretano a base di poliestere (PE-PUR) rispetto ad altri dispositivi che non la contengono.
Aggiornamento per i pazienti sull'Avviso di sicurezza

Scopri di più sul dispositivo sostitutivo
Domande e riposte
I prodotti elencati di seguito sono interessati dalla notifica di richiamo/avviso di sicurezza:
Dispositivi CPAP e PAP a due livelli
Avviso di sicurezza II Tutti i dispositivi interessati prodotti prima del 26 aprile 2021, tutti i numeri di serie dei dispositivi
Ventilazione a pressione continua, supporto ventilatorio minimo, uso presso la struttura
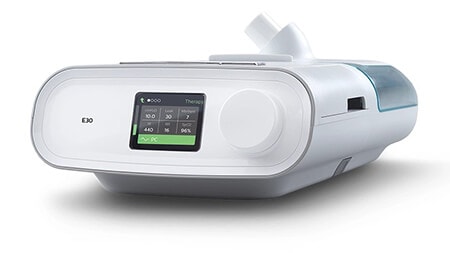
E30
(Approvazione in deroga per l'uso in situazioni di emergenza)

DreamStation ASV
Noto anche come DreamStation BiPAP autoSV

DreamStation ST, AVAPS
Noto anche come DreamStation BiPAP AVAPS, DreamStation BiPAP S/T

SystemOne ASV4
Noto anche come System One BiPAP autoSV, System One BiPAP autoSV Advanced

Serie C ASV, S/T, AVAPS
Noto anche come System One BiPAP ASV (C-Series), System One BiPAP AVAPS (C-Series),System One BiPAP S/T (C-Series)

OmniLab Advanced Plus
Dispositivo di titolazione in laboratorio

BiPAP Synchrony II
Legacy BiPAP

BiPAP ASV II & III
Legacy BiPAP

SystemOne (Serie Q)
noto anche come System One 50 series CPAP, Auto CPAP, BiPAP

REMStar SE Auto CPAP
noto anche come System One 60 series CPAP, Auto CPAP, BiPAP

DreamStation CPAP, Auto CPAP, BiPAP

DreamStation GO CPAP, APAP, Auto CPAP

Dorma 400, 500 CPAP, Auto CPAP
(non commercializzato negli Stati Uniti)
Se il tuo dispositivo è tra quello interessati...
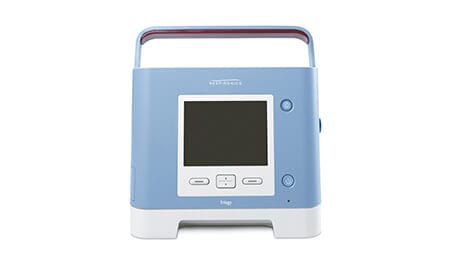
Trilogy 100
Ventilatore

Trilogy 200
Ventilatore

Garbin, Aeris 200, LifeVent
Ventilatori (non commercializzato negli Stati Uniti)
Ventilazione a pressione continua, supporto ventilatorio minimo, uso presso la struttura

A-Series BiPAP Hybrid A30
Noto anche come Ventilatore BiPAP Hybrid A30 (A-Series)
(non commercializzato negli Stati Uniti)

Ventilatore A-Series BiPAP V30 Auto
Noto anche come Ventilatore BiPAP V30 Auto (A-Series)
Ventilazione a pressione continua non di supporto vitale

A-Series BiPAP A40
Noto anche come Ventilatore BiPAP A40 (A-Series)
(non commercializzato negli Stati Uniti)

A-Series BiPAP A30
Noto anche come Ventilatore BiPAP A30(A-Series)
(non commercializzato negli Stati Uniti)
Se il tuo dispositivo è tra quello interessati...
Quali prodotti non sono interessati e perché?
I prodotti che non sono interessati potrebbero avere materiali in schiuma insonorizzanti diversi, perché nel tempo diventano disponibili nuovi materiali e tecnologie. Inoltre, la schiuma insonorizzante nei dispositivi non interessati può essere situata in una posizione diversa a causa del design del dispositivo.

